Co to reakcja ksantoproteinowa?
Reakcja ksantoproteinowa to reakcja charakterystyczna wykrywania białek za pomocą stężonego kwasu azotowego (V). Obecność białek (a, mówiąc precyzyjnie, aminokwasów posiadających pierścienie aromatyczne) wykrywa się poprzez pojawienie się żółtego zabarwienia w substancji. Dodatek NaOH powoduje pogłębienie barwy do pomarańczowej skutkiem utworzenia odpowiedniej soli w wyniku zachodzącej reakcji. Nazwa reakcji pochodzi od greckiego słowa ksanthôs, które oznacza żółty.
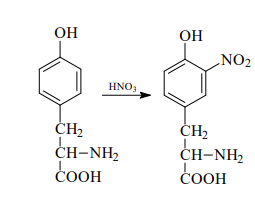
Podczas reakcji ksantoproteinowej dochodzi do nitrowania aromatycznych reszt aminokwasowych w aminokwasach tyrozynie, tryptofanie i fenyloalaninie, które w swojej budowie zawierają pierścień benzenowy. To właśnie nitrowany pierścień aromatyczny zabarwia się na żółto.
Aminokwasy aromatyczne znajdują się w wielu białkach, w tym w tych budujących skórę. Stąd pochodzi żółte zabarwienie skóry, gdy przez nieuwagę obleje się palce stężonym HNO3. Dodatnią próbę ksantoproteinową dają również związki aromatyczne (fenol, benzen) niezwiązane z białkami.
Jak przeprowadzić reakcję ksantroproteinową?
Reakcję ksantoproteinową można przeprowadzić dla próbek pochodzenia zwierzęcego i roślinnego. Aby zmiana zabarwienia była widoczna, najlepiej jest użyć produktów o jasnej barwie, np. białka jaja kurzego, jogurtu naturalnego, białej fasoli.
Materiał należy umieścić na szalce Petriego lub szkiełku zegarkowym i za pomocą pipety nanieść na niego kilka kropel stężonego HNO3. Na produktach, w których znajduje się białko, w miejscu kontaktu materiału z kwasem azotowym (V) pojawi się intensywnie żółte trwałe zabarwienie.