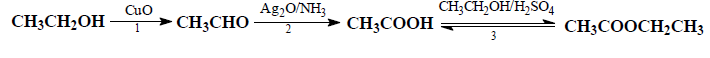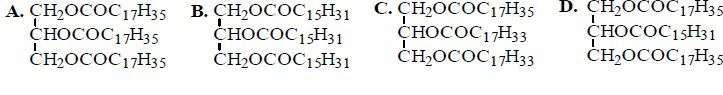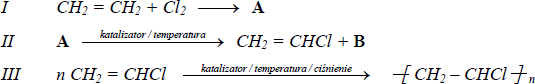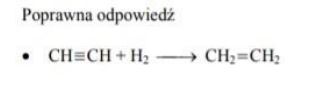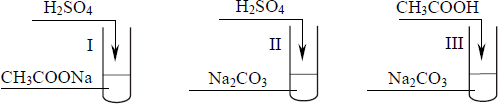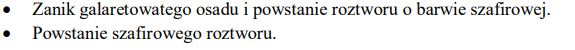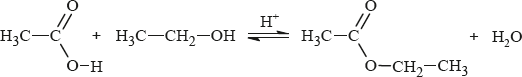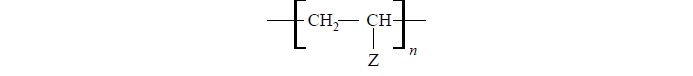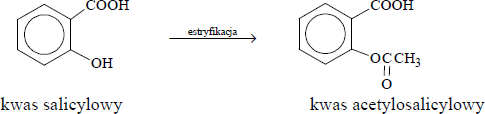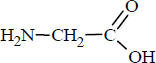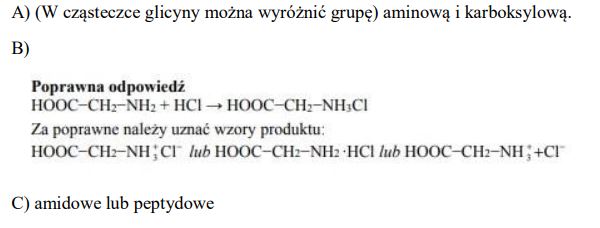Zadania maturalne z Chemii
Tematyka: tłuszcze, aminokwasy, peptydy, białka, cukry, izomeria optyczna.
Zadania pochodzą z oficjalnych arkuszy maturalnych CKE, które służyły przeprowadzaniu majowych egzaminów. Czteroznakowy kod zapisany przy każdym zadaniu wskazuje na jego pochodzenie: S/N – „stara”/”nowa” formuła; P/R – poziom podstawowy/rozszerzony; np. 08 – rok 2008.
Zbiór zadań maturalnych w formie arkuszy, możesz pobrać >> TUTAJ <<.
Zadanie 1. (SP05)
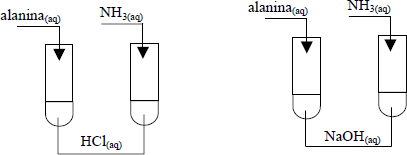
W celu zbadania właściwości chemicznych amoniaku i alaniny (kwasu 2-aminopropanowego) przeprowadzono doświadczenia przedstawione na poniższym rysunku. Podaj, który z badanych związków chemicznych reagował z kwasem i zasadą.
Odpowiedź słowną uzasadnij, zapisując równania odpowiednich reakcji w formie cząsteczkowej.
Alanina
Reakcja alaniny z kwasem :
CH3 – CH –COOH + HCl → CH3 – CH – COOH
| |
NH2 NH3Cl
Reakcja z zasadą :
CH3 – CH –COOH + NaOH→CH3 – CH – COONa + H2O
| |
NH2 NH2
Cząsteczka alaniny może być przedstawiona w formie jonu obojnaczego, a wzory produktów reakcji w postaci:
CH3 – CH – COOH CH3 – CH – COONa+
| |
NH3+ Cl– NH2
Zadanie 2. (SP05)
„ (…) Przekonanie, że należy unikać wszelkich tłuszczów, w dużym stopniu wynikało z obserwacji społeczeństw bogatych krajów zachodnich, gdzie ich spożycie jest znaczne i odnotowuje się dużą zapadalność na chorobę wieńcową. Jednak zależność ta dotyczy jedynie tłuszczów nasyconych. W społeczeństwach, w których konsumuje się stosunkowo dużo tłuszczów jedno- i wielonienasyconych, na tę chorobę zapada z reguły mniej osób. Na przykład tradycyjna dieta Kreteńczyków zawiera duże ilości oliwy (będącej bogatym źródłem tłuszczów jednonienasyconych) i ryb (bogatych w tłuszcze wielonienasycone). (…)”
Na podstawie: Czasopismo „Świat nauki” WSiP, nr 3 marzec 2003, 2. 46, 47.
Dokonaj analizy tego tekstu oraz
a) wymień jeden produkt spożywczy będący źródłem tłuszczów jednonienasyconych i jeden produkt spożywczy będący źródłem tłuszczów wielonienasyconych,
b) podaj nazwę przykładowego tłuszczu (jedno- lub wielonienasyconego), którego spożycie nie powoduje zwiększonej zapadalności na chorobę wieńcową.
- Oliwa
- Ryby
- trioleinian glicerolu
Zadanie 3. (SP05)
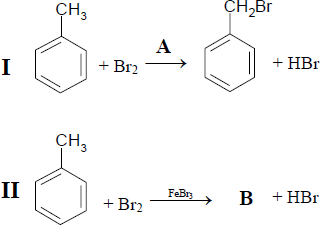
Metylobenzen (toluen) może reagować z bromem, tworząc w zależności od warunków różne produkty.
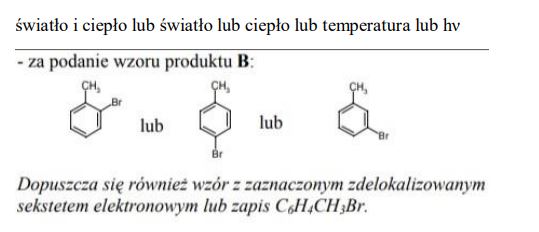
Analizując równania reakcji zapisane poniżej, określ warunki (A) reakcji I i podaj wzór jednego z możliwych produktów (B) reakcji II.
Zadanie 4. (SP05)
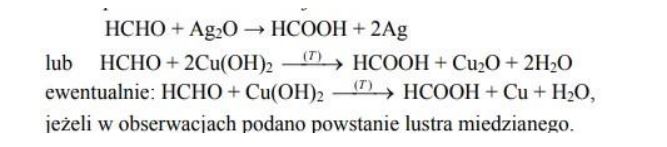
Formalina jest wodnym roztworem metanalu (aldehydu mrówkowego) o stężeniu ok. 40%. Zaprojektuj doświadczenie pozwalające zidentyfikować metanal (aldehyd mrówkowy) w formalinie.
Przedstaw schemat doświadczenia i oczekiwane obserwacje. Napisz równanie zachodzącej reakcji chemicznej.
Zadanie 5. (SP06)
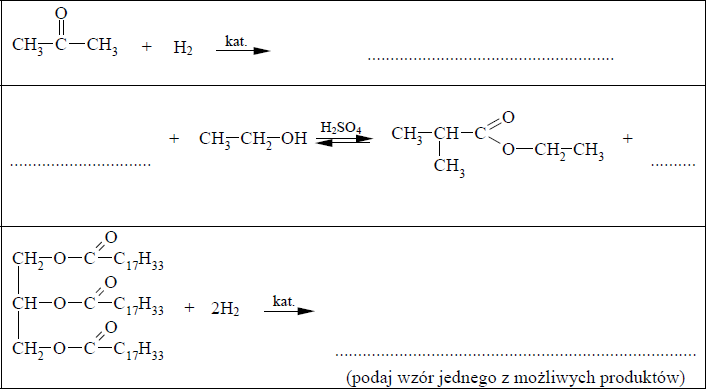
Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1).
a) Podaj nazwę systematyczną związku organicznego otrzymanego w tej
b) Określ, jaką rolę w tej reakcji pełni chlorek glinu.
Zadanie 6. (SP06)
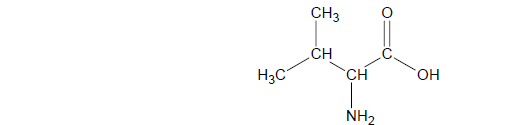
Poniższy rysunek przedstawia doświadczenie, które wykonano w celu odróżnienia roztworu wodnego glukozy od roztworu wodnego glicerolu (gliceryny). Przed ogrzaniem w obu probówkach niebieski osad wodorotlenku miedzi(II) rozpuścił się (roztworzył się) i powstał roztwór o szafirowym zabarwieniu. Po ogrzaniu w probówce A wytrącił się ceglasty osad, a w probówce B pojawił się osad o czarnym zabarwieniu.
a) Napisz, jaka cecha budowy cząsteczek glukozy i glicerolu (gliceryny) spowodowała powstanie szafirowego zabarwienia obu roztworów przed ich ogrzaniem.
b) Podaj nazwę substancji, której wodny roztwór znajdował się w probówce A i krótko uzasadnij swój wybór.
- A) Powstanie szafirowego zabarwienia jest spowodowane obecnością kilku grup hydroksylowych w cząsteczce glukozy i w cząsteczce glicerolu.
- B) W probówce A znajdował się wodny roztwór glukozy, która ma właściwości redukujące. W doświadczeniu zaszła redukcja miedzi(II) do miedzi(I). Ceglasty osad to tlenek miedzi(I).
Zadanie 7. (SP06)
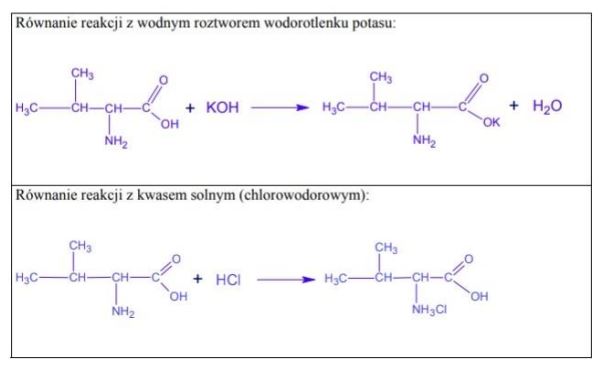
Jednym z aminokwasów białkowych jest walina o następującym wzorze:
Napisz w formie cząsteczkowej równania reakcji waliny z wodnym roztworem wodorotlenku potasu i kwasem solnym (chlorowodorowym).Zastosuj wzory półstrukturalne (grupowe) związków organicznych. Równanie reakcji z wodnym roztworem wodorotlenku potasu: Równanie reakcji z kwasem solnym (chlorowodorowym):
Zadanie 8. (SP07)
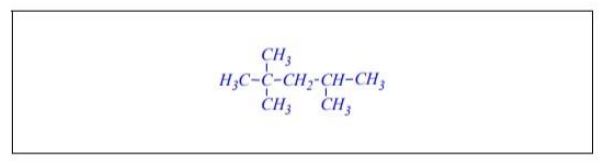
Przedstaw wzór półstrukturalny (grupowy) 2,2,4-trimetylopentanu.
Zadanie 9. (SP07)
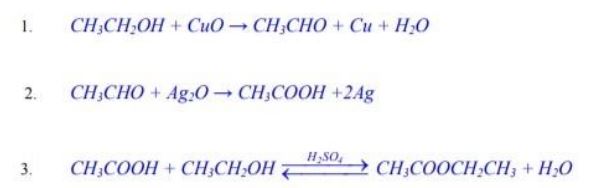
Stosując wzory półstrukturalne (grupowe) związków organicznych, napisz równania kolejnych reakcji (1-3) zachodzących zgodnie z poniższym schematem.
Zadanie 10. (SP07)
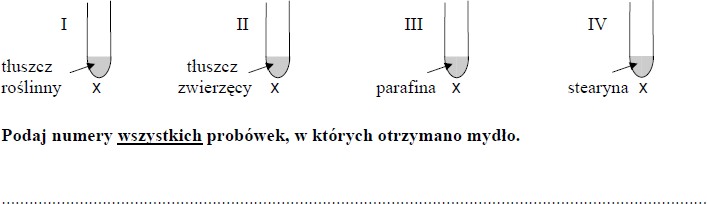
Do probówek oznaczonych numerami I – IV, zawierających substancje organiczne, dodano zasadę sodową. Zawartość każdej z probówek ogrzano.
Podaj numery wszystkich probówek, w których otrzymano mydło.
I, II oraz IV
Zadanie 11. (SP07)
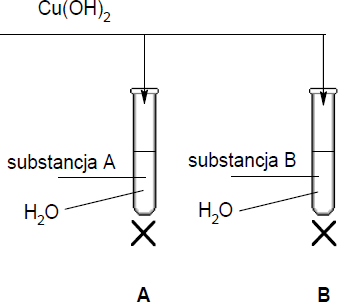
Do naczynia zawierającego tłuszcz dodano wodę bromową. Zawartość naczynia wstrząśnięto i zaobserwowano, że woda bromowa odbarwiła się. Wskaż wzór tłuszczu, który znajdował się w naczyniu.
Zadanie 12. (SP07)
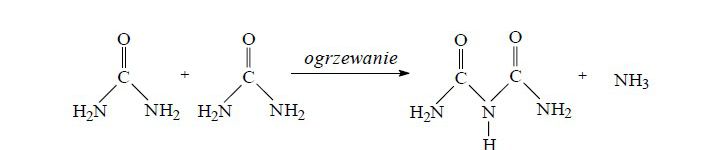
Mocznik podczas ogrzewania ulega reakcji przedstawionej równaniem:
Fragment cząsteczki organicznego produktu powyższej reakcji stanowi wiązanie występujące między innymi w białkach.
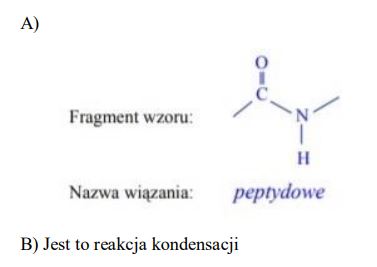
a) Narysuj ten fragment wzoru cząsteczki i podaj nazwę tego wiązania.
b) Określ, czy przedstawiona w informacji reakcja jest reakcją typu substytucji, kondensacji czy polimeryzacji.
Zadanie 13. (SP08)
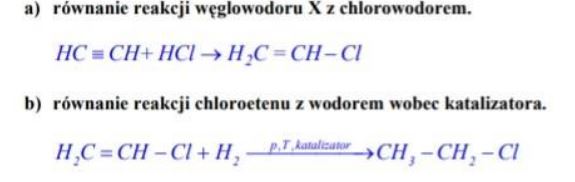
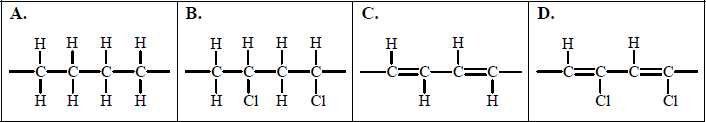
W wyniku reakcji addycji chlorowodoru do węglowodoru X powstaje chloroeten (chlorek winylu) o wzorze H2C=CH-Cl.
Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych,
a) równanie reakcji węglowodoru X z chlorowodorem
b) równanie reakcji chloroetenu z wodorem wobec
Zadanie 14. (SP08)
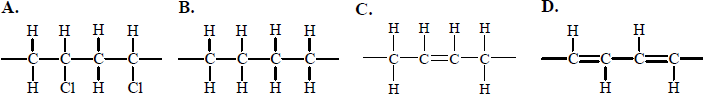
Chloroeten ma zdolność ulegania reakcji polimeryzacji. Spośród poniżej przedstawionych wzorów wybierz ten, który ilustruje budowę fragmentu łańcucha produktu polimeryzacji chloroetenu (chlorku winylu). Zaznacz odpowiedź A, B, C lub D.
Zadanie 15. (SP08)
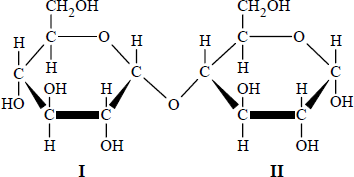
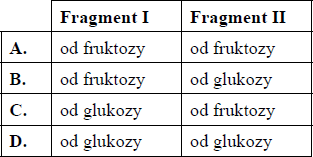
Poniżej przedstawiono wzór pewnego dwucukru.
Określ, od jakich cukrów prostych pochodzą fragmenty I i II, z których zbudowana jest cząsteczka tego dwucukru. Zaznacz odpowiedź A, B, C lub D.
- od glukozy , od glukozy
Zadanie 16. (SP09)
Polichlorek winylu (PVC) otrzymuje się z etenu i chloru w procesie, który można przedstawić za pomocą poniższych schematów reakcji I i II oraz równania reakcji III.
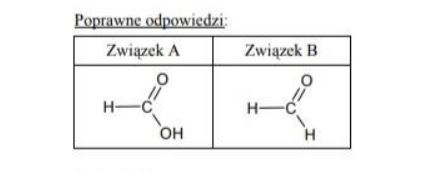
a) Dokonaj analizy schematów i podaj wzór półstrukturalny (grupowy) substancji A oraz wzór substancji Wzór półstrukturalny (grupowy) substancji A: Wzór substancji B:
b) Określ typy reakcji I i II, posługując się podziałem charakterystycznym dla chemii
A)
A: CH2Cl – CH2Cl
B: HCl
B)
Typ reakcji I: reakcja addycji
Typ reakcji II: reakcja eliminacji
Zadanie 17. (SP09)
W poniższej tabeli opisano właściwości dwóch związków organicznych zawierających taką samą liczbę atomów węgla w cząsteczce, ale należących do różnych grup jednofunkcyjnych pochodnych węglowodorów.
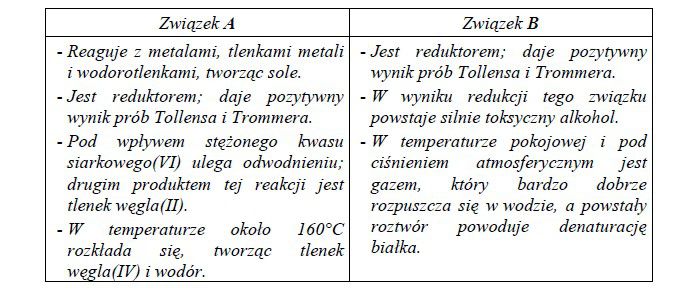
Zadanie 18. (SP09)
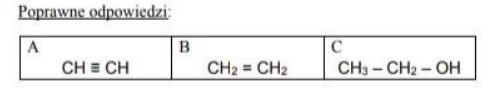
Węgliku wapnia użyto jako surowca w procesie, którego schemat przedstawiono poniżej.
Uwaga: związek B powstaje w reakcji związku A z wodorem w stosunku molowym 1:1.
Podaj wzory półstrukturalne (grupowe) związków organicznych A, B i C.
Zadanie 19. (SP09)
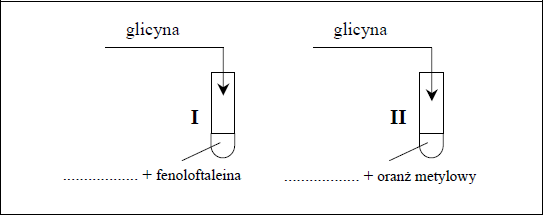
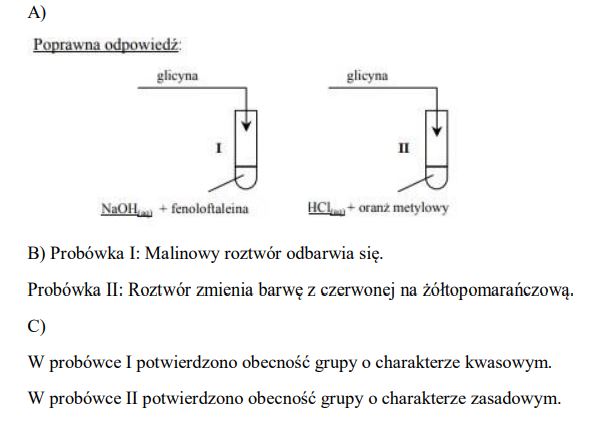
Przedstaw projekt doświadczenia, które wykaże, że kwas aminooctowy (glicyna) zawiera w cząsteczce grupę funkcyjną o charakterze kwasowym (karboksylową) oraz grupę funkcyjną o charakterze zasadowym (aminową). W tym celu:
a) Uzupełnij poniższy opis doświadczenia, wpisując wzory potrzebnych odczynników wybranych spośród:
HCl(aq), CuSO4(aq), I2 w KI(aq), NaOH(aq), Cu(OH)2(zawiesina)
b) Wymień obserwacje, które umożliwią określenie charakteru chemicznego grup funkcyjnych w cząsteczce glicyny (uwzględnij zmianę barwy roztworów).
c) Określ charakter chemiczny grup funkcyjnych, których obecność potwierdzono, wykonując doświadczenie.
W probówce I potwierdzono obecność grupy o charakterze: ………………………………………..
W probówce II potwierdzono obecność grupy o charakterze: ……………………………………….
Zadanie 20. (SP10)
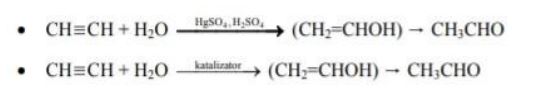
Ważną reakcją, której ulega etyn (acetylen), jest przyłączanie wody. Przemiana ta zachodzi w obecności mieszaniny H2SO4 i HgSO4 jako katalizatora. Produktem tej reakcji jest aldehyd zawierający dwa atomy węgla w cząsteczce.
Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie opisanej przemiany.
W równaniu nad strzałką napisz warunki, w jakich zachodzi ta reakcja.
Zadanie 21. (SP10)
Poniższy schemat ilustruje ciąg przemian, których początkowym substratem jest etyn (acetylen):
etyn (acetylen) →1 eten →2 polimer
Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie reakcji oznaczonej na schemacie numerem 1.
Zadanie 22. (SP10)
Poniższy schemat ilustruje ciąg przemian, których początkowym substratem jest etyn (acetylen):
etyn (acetylen) →1 eten →2 polimer
Spośród przedstawionych poniżej wzorów podkreśl ten, który przedstawia budowę fragmentu łańcucha polimeru stanowiącego produkt reakcji oznaczonej na schemacie numerem 2.
Zadanie 23. (SP10)
Kwasy tłuszczowe o wzorach C17H35COOH (kwas stearynowy) i C17H33COOH (kwas oleinowy) należą do różnych szeregów homologicznych.
Określ różnicę w budowie cząsteczek tych związków. W tym celu w każdym nawiasie wybierz i podkreśl właściwe określenie.
Kwas oleinowy, w przeciwieństwie do kwasu stearynowego, jest kwasem (nasyconym / nienasyconym). W cząsteczce kwasu stearynowego pomiędzy atomami węgla (występuje jedno wiązanie podwójne / występują tylko wiązania pojedyncze).
Kwas oleinowy, w przeciwieństwie do kwasu stearynowego, jest kwasem nienasyconym. W cząsteczce kwasu stearynowego pomiędzy atomami węgla występują tylko wiązania pojedyncze.
Zadanie 24. (SP10)
Kwasy tłuszczowe o wzorach C17H35COOH (kwas stearynowy) i C17H33COOH (kwas oleinowy) należą do różnych szeregów homologicznych.
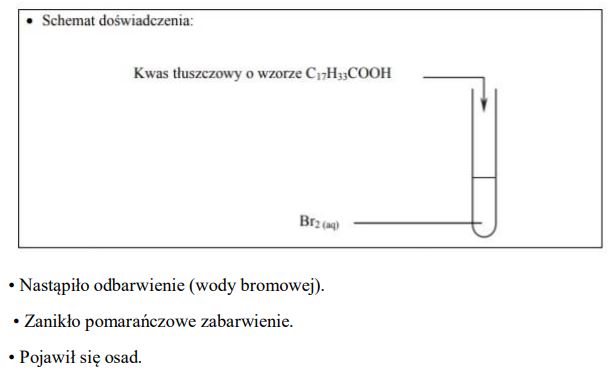
Zaprojektuj doświadczenie, którego przebieg pozwoli potwierdzić nienasycony charakter kwasu tłuszczowego.
a) Uzupełnij schemat doświadczenia, wpisując wzory odczynników wybranych z poniższej listy:
C17H33COOH • C17H35COOH • Br2 (aq) • NaOH (aq) • FeCl3 (aq)

Zadanie 25. (SP10)
Przeanalizuj poniższe schematy przedstawiające trzy reakcje chemiczne i wpisz wzory brakujących substratów lub produktów. Związki organiczne przedstaw za pomocą wzorów półstrukturalnych (grupowych).
Zadanie 26. (SP10)
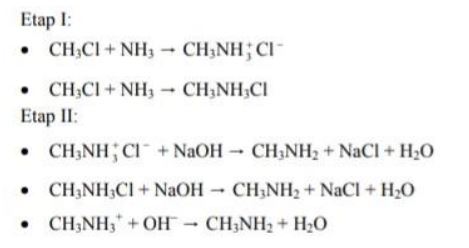
Aminy alifatyczne otrzymuje się w reakcji chlorowcopochodnych węglowodorów z amoniakiem. Przemianę tę przeprowadza się dwuetapowo. W pierwszym etapie powstaje sól amoniowa RNH + 3 Cl − . W drugim etapie powstałą sól poddaje się działaniu NaOH.
Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równania reakcji przedstawiające dwuetapowy proces otrzymywania metyloaminy.
Zadanie 27. (SP10)
Oceń prawdziwość poniższych zdań i uzupełnij tabelę. Wpisz literę P, jeżeli uznasz zdanie za prawdziwe, lub literę F, jeżeli uznasz je za fałszywe.
PFP
Zadanie 28. (SP11)
W probówce I wyczuwało się charakterystyczny zapach octu.
W probówce II i III reakcje przebiegły gwałtownie i wydzielił się bezbarwny gaz.
a) Na podstawie informacji wprowadzającej uzupełnij poniższe zdanie. W każdym nawiasie wybierz i podkreśl nazwę właściwego kwasu.
Najmocniejszym kwasem jest kwas (etanowy / siarkowy(VI) / węglowy), a najsłabszym kwasem jest kwas (etanowy / siarkowy(VI) / węglowy).
b) Napisz w formie cząsteczkowej równania reakcji zachodzących w probówkach I i II.
c) Powstający w probówce III bezbarwny gaz wprowadzono do zlewki, w której znajdował się wodny roztwór wodorotlenku wapnia.
I. Napisz, co zaobserwowano podczas tego doświadczenia.
II. Przedstaw w formie cząsteczkowej równanie reakcji zachodzącej w zlewce.
Zadanie 29. (SP11)
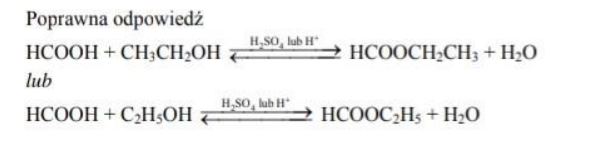
Pewien związek organiczny w obecności kwasu siarkowego(VI) reaguje z etanolem, dając substancję chemiczną o wzorze sumarycznym C3H6O2. Substancja ta ma charakterystyczny zapach.
Drugim produktem reakcji jest woda.
Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie opisanej przemiany. W równaniu nad strzałką napisz warunki, w jakich zachodzi ta reakcja.
Zadanie 30. (SP11)
Oceń prawdziwość poniższych zdań i uzupełnij tabelę. Wpisz literę P, jeżeli uznasz zdanie za prawdziwe, lub literę F, jeżeli uznasz je za fałszywe.
FPP
Zadanie 31. (SP11)
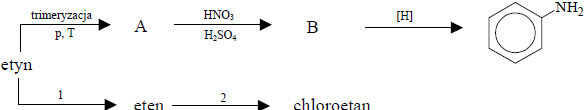
Poniższy schemat ilustruje ciąg przemian chemicznych.
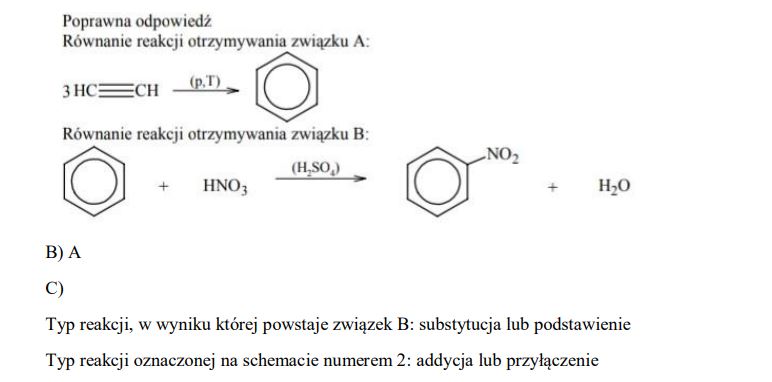
a) Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie reakcji otrzymywania związku A z etynu oraz równanie reakcji otrzymywania związku B ze związku A.
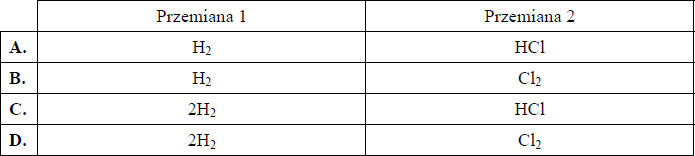
b) Jeden mol etynu poddano przemianom prowadzącym do powstania chloroetanu. Korzystając z informacji, wybierz i podkreśl wiersz A–D, w którym poprawnie zapisano wzory i liczby moli nieorganicznych substratów przemian oznaczonych na schemacie numerami 1 i 2.
c) Posługując się podziałem charakterystycznym dla chemii organicznej, określ typ reakcji, w wyniku której powstaje związek B, oraz typ reakcji oznaczonej na schemacie numerem 2.
Zadanie 32. (SP11)
Aminokwasy wchodzące w skład białek noszą nazwy zwyczajowe i często oznaczane są trzyliterowymi symbolami stosowanymi do zwięzłego zapisywania struktury białek, np. glicyna (Gly), alanina (Ala). Jeżeli w reakcji kondensacji uczestniczą te dwa aminokwasy, to w produktach reakcji można wykryć cztery rodzaje dipeptydów zapisanych umownie: Gly-Ala, Ala-Gly, Gly-Gly i Ala-Ala.
Podaj liczbę łańcuchowych tripeptydów, które mogą powstać w wyniku kondensacji zachodzącej w mieszaninie glicyny (Gly) i seryny (Ser).
Liczba możliwych tripeptydów: 8
Zadanie 33. (SP11)
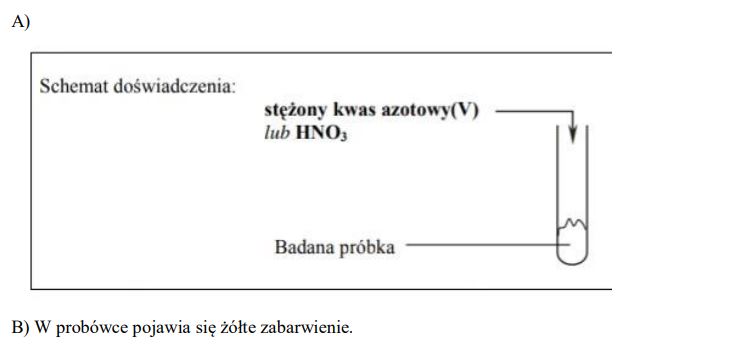
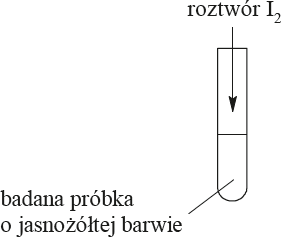
Białka stanowią podstawowy budulec wszystkich organizmów, są składnikiem włókien naturalnych pochodzenia zwierzęcego, np. wełny i jedwabiu naturalnego. W probówce znajduje się biała próbka
jedwabiu naturalnego.
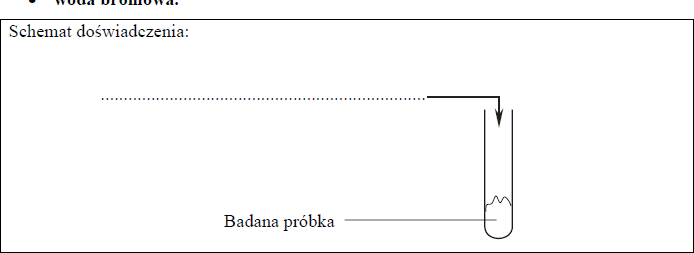
Zaprojektuj doświadczenie, które potwierdzi obecność białka w badanej próbce.
a) Uzupełnij schemat doświadczenia, wpisując nazwę odczynnika wybranego z listy:
wodny roztwór manganianu(VII) potasu
• stężony kwas azotowy(V)
• woda bromowa.
b) Napisz, co zaobserwowano podczas tego doświadczenia.
Zadanie 34. (SP11)
Pomysł otrzymania tworzyw o strukturze polimerowej zawdzięczamy analizie budowy naturalnych polimerów, takich jak kauczuk czy wełna. Wyróżnia się polimery addycyjne oraz polimery kondensacyjne. Polimery addycyjne powstają wtedy, gdy w reakcji następuje łączenie się monomerów bez równoczesnego wydzielania się cząsteczek produktu ubocznego. Polimery kondensacyjne powstają w reakcjach, w których oprócz polimeru wydzielają się niewielkie cząsteczki produktu ubocznego, którym najczęściej jest woda. Poniżej przedstawione są dwie przemiany chemiczne:
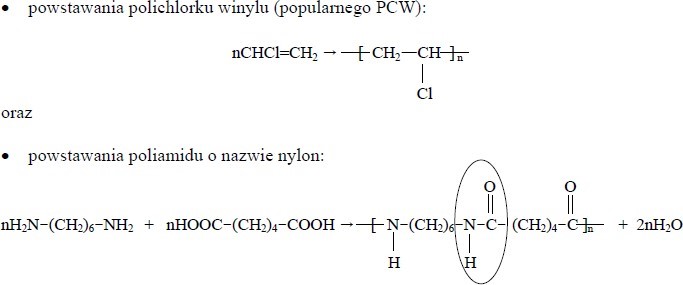
1. polichlorek winylu
2. nylon.
b) Podaj nazwę zaznaczonego wiązania, które występuje w polimerze o nazwie
A)
Polichlorek winylu: (polimer) addycyjny
Nylon: (polimer) kondensacyjny
B)
peptydowe lub amidowe
Zadanie 35. (SP11)
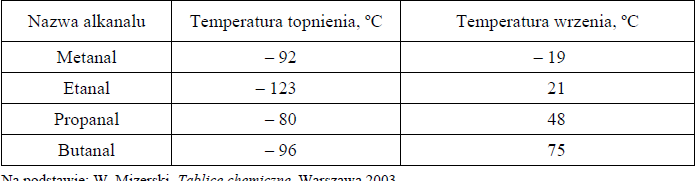
W tabeli przedstawiono wybrane właściwości alkanali (pod ciśnieniem 1013 hPa).
Korzystając z powyższej tabeli, określ stan skupienia
a) metanalu oraz etanalu w warunkach normalnych.
b) propanalu oraz butanalu w temperaturze – 90 ºC i pod ciśnieniem 1013 hPa.
- A) Metanal: gaz
Etanal: ciecz
- B) Propanal: ciało stałe
Butanal: ciecz
Zadanie 36. (SP12)
W oddzielnych probówkach przygotowano wodne roztwory następujących substancji i zbadano ich przewodnictwo elektryczne oraz odczyn otrzymanych roztworów.
Oceń prawdziwość poniższych zdań. Wpisz do tabeli literę P, jeżeli zdanie jest prawdziwe, lub F jeśli jest fałszywe.
PFP
Zadanie 37. (SP12)
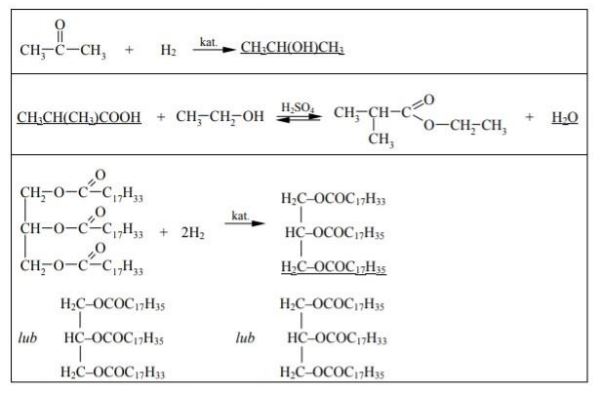
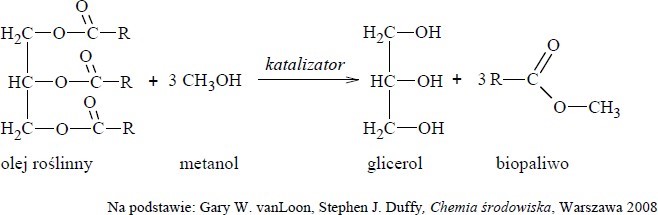
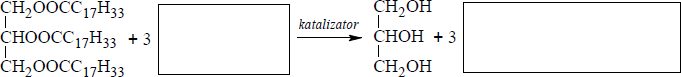
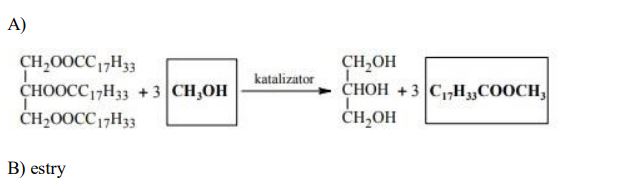
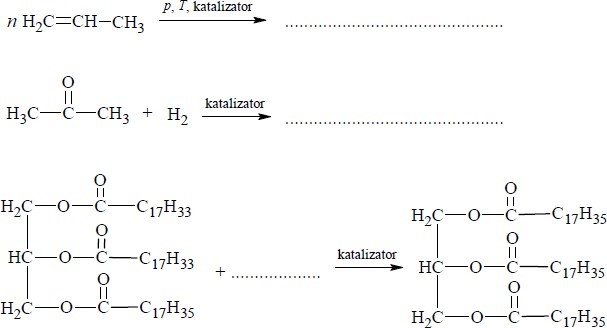
Paliwa do silników wysokoprężnych otrzymywane z ropy naftowej można zastąpić biopaliwami. Wytwarzanie biopaliwa polega na ogrzewaniu oleju roślinnego z dużą ilością alkoholu w obecności katalizatora. Proces ten można zilustrować ogólnym równaniem, w którym R oznacza grupę węglowodorową:
a) Uzupełnij poniższy schemat równania reakcji otrzymywania biopaliwa z trioleinianu glicerolu i metanolu, wpisując wzory półstrukturalne (grupowe) brakującego substratu i produktu.
b) Napisz nazwę grupy jednofunkcyjnych pochodnych węglowodorów, do której zalicza się główny składnik biopaliwa otrzymanego opisaną metodą.
Zadanie 38. (SP12)
Uzupełnij poniższą charakterystykę glicerolu (propano-1,2,3-triolu), wybierając jedno określenie spośród podanych w każdym nawiasie. Wybrane określenia podkreśl.
Glicerol reaguje z aktywnymi metalami, np. z sodem, tworząc alkoholany i (wodór / wodę), pod działaniem kwasów karboksylowych (ulega / nie ulega) reakcji estryfikacji, a w reakcji z wodorotlenkiem miedzi(II) tworzy (czarny osad / pomarańczowy osad / szafirowy roztwór).
Glicerol reaguje z aktywnymi metalami, np. z sodem, tworząc alkoholany i wodór , pod działaniem kwasów karboksylowych ulega reakcji estryfikacji, a w reakcji z wodorotlenkiem miedzi(II) tworzy szafirowy roztwór.
Zadanie 39. (1 pkt) 13PS
Poniższy schemat ilustruje ciąg przemian chemicznych.
W przemianie oznaczonej numerem 1 stosunek molowy gazowych reagentów A i H2 wynosi = A H2 n 1 : 2.
Produktem tej reakcji jest związek nasycony B.
W przemianie oznaczonej numerem 2 powstaje monochloropochodna, z której w kolejnej przemianie powstaje związek nienasycony D. Ostatni etap (przemiana oznaczona numerem 4) prowadzi do otrzymania związku wielkocząsteczkowego.
a) Podaj nazwę szeregu homologicznego, do którego należy związek A, oraz nazwę szeregu homologicznego, do którego należy związek B.
b) Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie reakcji oznaczonej na schemacie numerem 3 oraz równanie reakcji oznaczonej na schemacie numerem 4.
c) Uzupełnij poniższe zdania. Wybierz i podkreśl właściwe określenie spośród podanych w każdym nawiasie.
Polietylen jest (reaktywnym / niereaktywnym) związkiem organicznym używanym do produkcji artykułów codziennego użytku. Jest tworzywem (palnym / niepalnym), które charakteryzuje się podatnością na barwienie i formowanie.
Zadanie 40. (SP13)
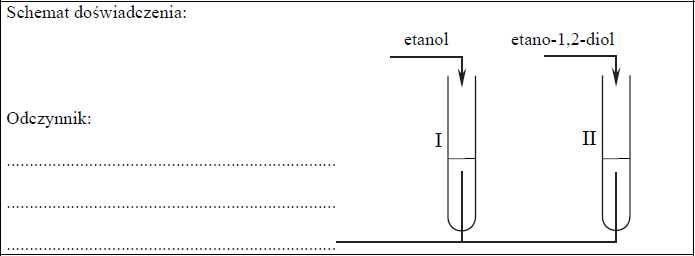
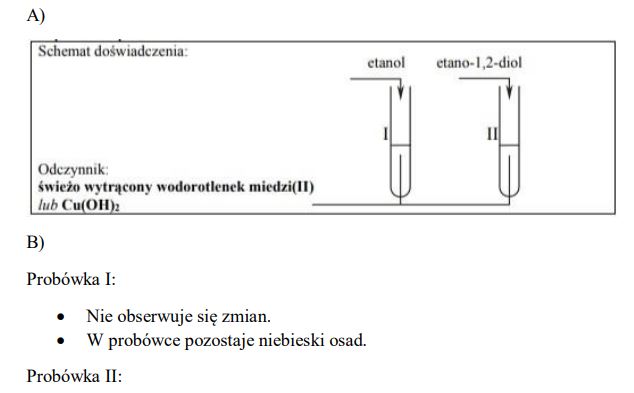
Zaprojektuj doświadczenie, które pozwoli odróżnić alkohol monohydroksylowy o wzorze CH3─CH2─OH od alkoholu polihydroksylowego o wzorze CH2(OH)─CH2(OH).
a) Uzupełnij schemat doświadczenia, wpisując nazwę użytego odczynnika wybranego z podanej listy:
1. świeżo wytrącony wodorotlenek miedzi(II)
2. wodny roztwór chlorku żelaza(III)
3. kawałeczek sodu.
b) Napisz, jakie obserwacje potwierdzą, że do probówki I wprowadzono etanol, a do probówki II etano-1,2-diol.
Zadanie 41. (SP13)
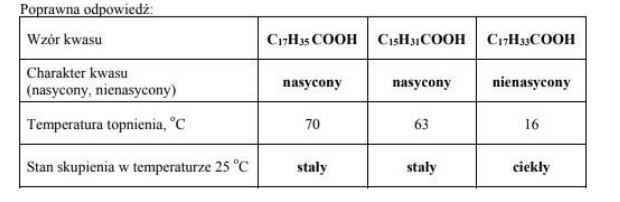
Dane są wzory trzech kwasów karboksylowych: C17H33COOH, C17H35COOH, C15H31COOH oraz zestawione w poniższej tabeli wartości ich temperatury topnienia.
Porównaj budowę kwasów o podanych powyżej wzorach i uzupełnij tabelę.
Zadanie 42. (SP13)
W wyniku reakcji etanolu z nasyconym kwasem monokarboksylowym, prowadzonej w obecności kwasu siarkowego(VI), tworzy się ester, w którego cząsteczce stosunek liczby atomów węgla do liczby atomów tlenu wynosi 2 : 1.
a) Ustal liczbę atomów węgla w cząsteczce opisanego estru
b) Napisz, stosując wzory półstrukturalne (grupowe) związków organicznych, równanie opisanej przemiany. W równaniu zaznacz warunki, w jakich zachodzi ta
Zadanie 43. (SP13)
Poniższy schemat ilustruje ciąg przemian chemicznych.
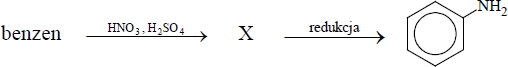
PPF
Zadanie 44. (SP14)
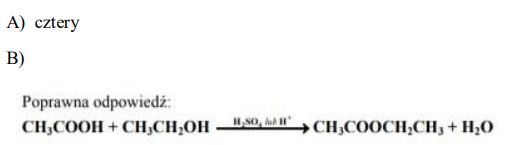
Reakcja kwasu etanowego (octowego) z etanolem przebiega według równania:
Reakcja ta zachodzi w obecności mocnego kwasu, np. kwasu siarkowego(VI).
Podaj nazwę estru powstającego w tej reakcji.
etanian etylu lub octan etylu
Zadanie 45. (SP14)
Poniżej przedstawiono schemat cyklu przemian, jakim ulegają metanol i jego pochodne.
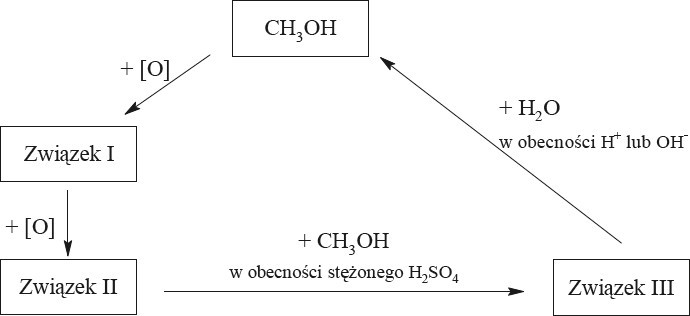
Wypełnij tabelę, wpisując wzory półstrukturalne (grupowe) pochodnych metanolu CH3OH, które na schemacie oznaczono numerami I–III.
Zadanie 46. (SP14)
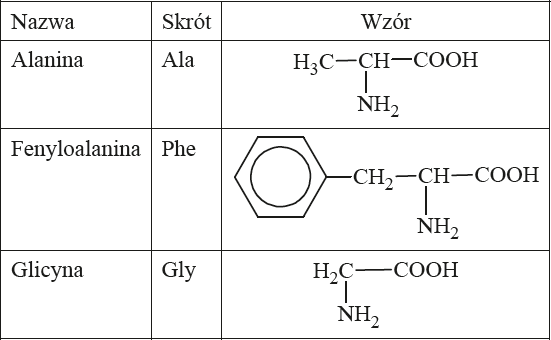
Tabela przedstawia nazwy, skróty nazw i wzory trzech aminokwasów.
Sekwencję (kolejność) aminokwasów w peptydach wyraża się, zapisując w odpowiedniej kolejności trzyliterowe skróty nazw aminokwasów, z których peptyd powstał. Reszta aminokwasu, którego skrót jest zapisany po lewej stronie, ma w peptydzie wolną grupę aminową, a reszta aminokwasu, którego skrót nazwy jest zapisany po prawej stronie, ma wolną grupę karboksylową.
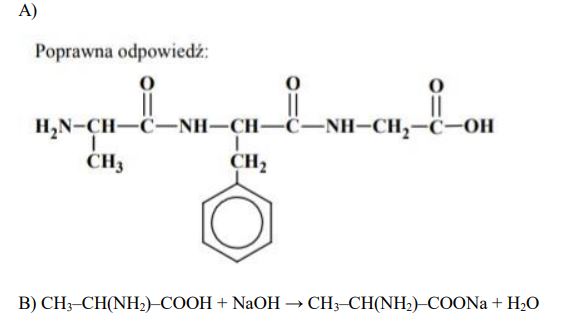
a) Napisz wzór półstrukturalny (grupowy) tripeptydu utworzonego z alaniny, fenyloalaniny i glicyny, w którym sekwencja reszt aminokwasów jest następująca: Ala-Phe-Gly.
b) Napisz w formie cząsteczkowej równanie reakcji alaniny z wodorotlenkiem sodu. Zastosuj wzory półstrukturalne (grupowe) reagentów organicznych.
c) Spośród aminokwasów wymienionych w tabeli wybierz ten, który ulega reakcji nitrowania. Napisz jego nazwę.
Zadanie 47. (SP14)
W celu sprawdzenia obecności skrobi w badanej próbce przygotowanej z nasion pewnej rośliny wykonano eksperyment, którego przebieg przedstawiono na rysunku.
Po dodaniu kropli odczynnika o ciemnobrunatnej barwie zawartość probówki zabarwiła się na granatowo. Sformułuj wniosek o obecności skrobi w badanej próbce.
(Badana próbka) zawierała skrobię.
Zadanie 48. (SP15)
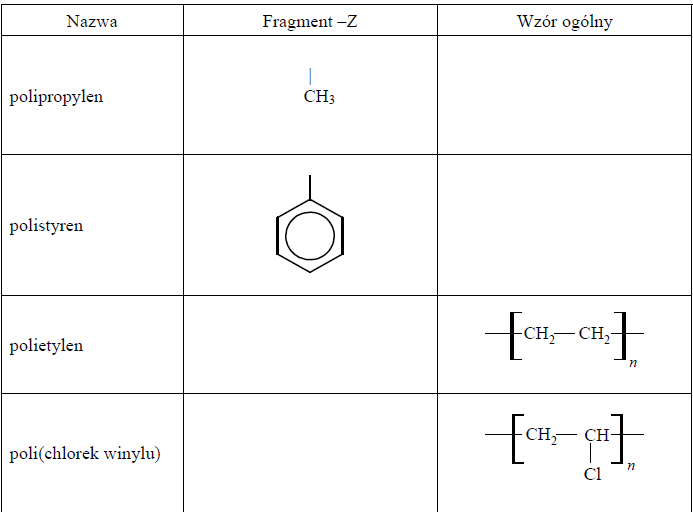
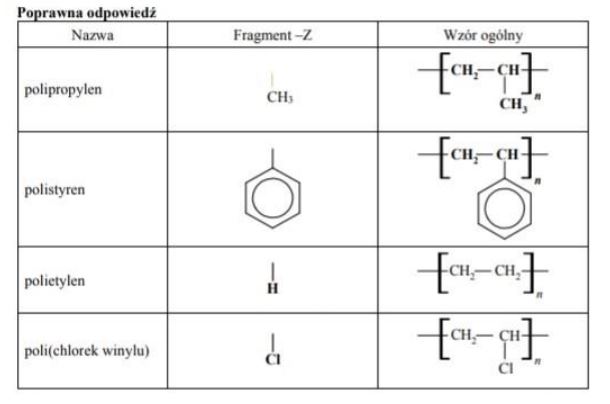
Tworzywa polimerowe wymienione w poniższej tabeli można przedstawić w następujący sposób (fragment –Z oznacza łańcuch boczny, atom wodoru lub atom chlorowca):
Uzupełnij tabelę – wpisz brakujące wzory fragmentów –Z lub wzory ogólne polimerów.
Zadanie 49. (SP15)
Kwas mlekowy powstaje między innymi w wyniku fermentacji fruktozy C6H12O6 − jako jedyny produkt tego procesu.
Napisz równanie reakcji fermentacji mleczanowej fruktozy. Zastosuj wzór półstrukturalny (grupowy) kwasu mlekowego.
Zadanie 50. (SP15)
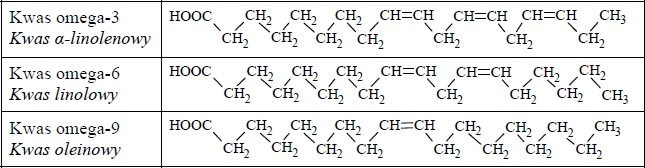
Nienasycone kwasy tłuszczowe, NNKT, to kwasy, które nie są syntezowane w organizmie człowieka i muszą być dostarczane wraz z pożywieniem. Zalicza się do nich kwasy omega-3, omega-6 oraz omega-9. Poniżej wymieniono przykłady NNKT.
a) Znajdź i opisz związek między numerem w nazwie kwasu omega (-3, -6, -9) a budową jego cząsteczki.
b) Głównymi składnikami oliwy z oliwek są triglicerydy kwasów tłuszczowych, przede wszystkim kwasu oleinowego oraz innych nienasyconych kwasów tłuszczowych. Zaprojektuj doświadczenie, dzięki któremu można wykazać nienasycony charakter reszt kwasów tłuszczowych obecnych w oliwie z oliwek.
I. Uzupełnij schemat doświadczenia. Wpisz nazwę użytego odczynnika wybranego spośród podanych poniżej:
− fenoloftaleina
− zasada sodowa
− woda bromowa
− wodny roztwór bromku potasu.
II. Napisz, jakie obserwacje potwierdzą nienasycony charakter reszt kwasów tłuszczowych obecnych w oliwie z oliwek.
c) Napisz wzór półstrukturalny (grupowy) cząsteczki triglicerydu kwasu oleinowego (trioleinianu glicerolu). Grupy węglowodorowe kwasu oleinowego zapisz w formie sumarycznej: –C17H33.
Zadanie 51. (SP16)
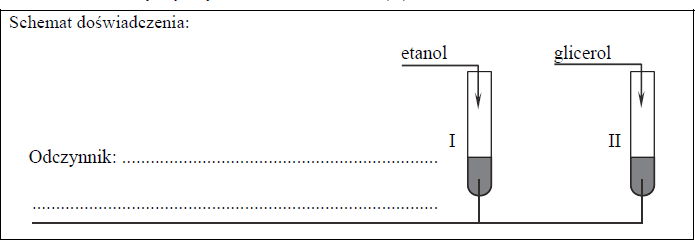
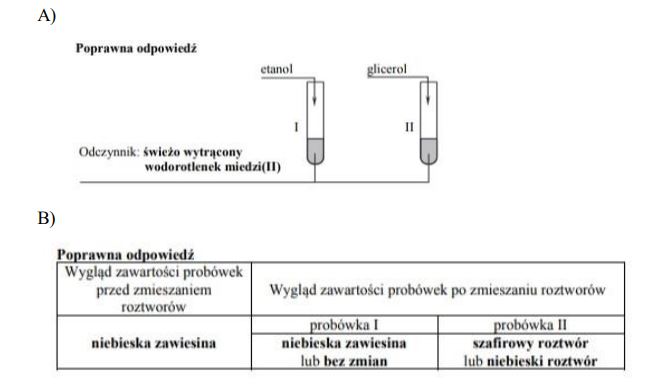
Zaprojektuj doświadczenie, którego przebieg umożliwi odróżnienie etanolu od glicerolu (propano- 1,2,3-triolu).
a) Uzupełnij schemat doświadczenia. Wpisz nazwę odczynnika wybranego spośród następujących:
− woda bromowa
− świeżo wytrącony wodorotlenek miedzi(II)
b) Opisz obserwowane w czasie doświadczenia zmiany, potwierdzające obecność etanolu w probówce I i glicerolu w probówce II (uzupełnij tabelę).
Zadanie 52. (SP16)
Kwas acetylosalicylowy (znany pod handlową nazwą „aspiryna”) to pochodna kwasu salicylowego, którą można otrzymać w wyniku przemiany opisanej poniższym schematem.
Oceń, czy poniższe informacje są prawdziwe. Zaznacz P, jeśli informacja jest prawdziwa, albo F – jeśli jest fałszywa.
FPP
Zadanie 53. (SP16)
Przeanalizuj poniższe schematy trzech reakcji chemicznych i wpisz brakujące wzory oraz uzupełnij współczynniki stechiometryczne. Związki organiczne przedstaw za pomocą wzorów półstrukturalnych (grupowych).
Zadanie 54. (SP16)
Glukoza jest syntetyzowana przez rośliny zielone podczas procesu fotosyntezy, w którym światło słoneczne dostarcza energię niezbędną do wytworzenia tego monosacharydu. Wiele cząsteczek glukozy łączy się następnie wiązaniami chemicznymi, w wyniku czego tworzy materiał budulcowy lub zapasowy rośliny.
Organizm ludzki nie wytwarza enzymów koniecznych do trawienia celulozy, więc dla człowieka źródłem węglowodanów jest skrobia. Jest ona trawiona w ustach i żołądku przez enzymy glikozydazy, w których obecności rozkłada się na glukozę. Na podstawie: John McMurry, Chemia organiczna, Warszawa 2000.
a) Określ, czy reakcja fotosyntezy jest endoenergetyczna, czy – egzoenergetyczna.
b) Uzupełnij poniższe zdanie – określ funkcję, jaką glikozydazy pełnią w opisanej reakcji rozkładu skrobi (podkreśl wybraną nazwę).
Glikozydazy pełnią w tej reakcji funkcję (katalizatora / substratu / produktu).
- A) endoenergetyczna
- B) Glikozydazy pełnią w tej reakcji funkcję katalizatora.
Zadanie 55. (SP17)
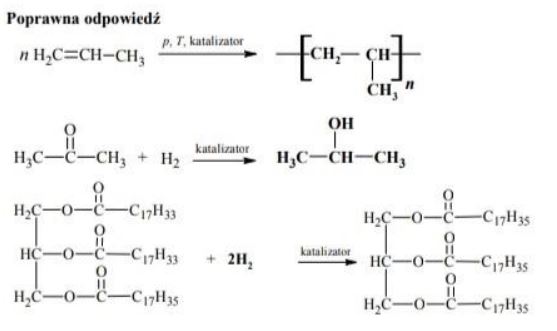
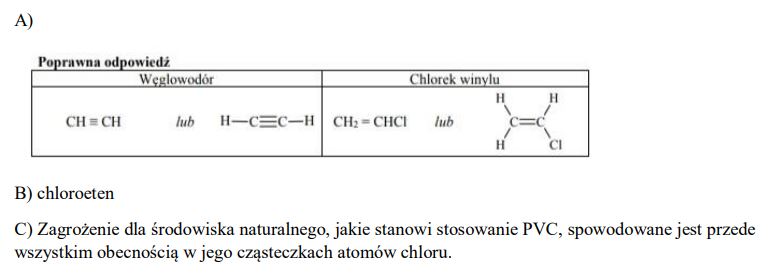
Poli(chlorek winylu), PVC, jest tworzywem sztucznym otrzymywanym w wyniku polimeryzacji chlorku winylu, który powstaje w reakcji addycji chlorowodoru do pewnego węglowodoru. Ten proces zilustrowano poniższym schematem.
a) Napisz wzór półstrukturalny (grupowy) węglowodoru, z którego otrzymuje się chlorek winylu, oraz wzór półstrukturalny (grupowy) chlorku winylu.
b) Napisz nazwę systematyczną chlorku winylu.
c) Obecnie obserwuje się spadek zastosowania poli(chlorku winylu) z powodu zagrożenia, jakie tworzywo to stanowi dla środowiska naturalnego. W ograniczonym stopniu nadaje się do przeróbki wtórnej, a podczas spalania odpadów z PVC wydzielają się toksyczne substancje.
Wybierz i podkreśl w każdym nawiasie poprawne uzupełnienie poniższego zdania.
Zagrożenie dla środowiska naturalnego, jakie stanowi stosowanie PVC, spowodowane jest przede wszystkim obecnością w jego cząsteczkach atomów (chloru / węgla / wodoru).
Zadanie 56. (SP17)
Do probówki I wprowadzono próbkę tristearynianu glicerolu, a do probówki II – próbkę trioleinianu glicerolu. Następnie do obu probówek dodano wodę bromową i zawartość każdej probówki wstrząśnięto.

Przykłady poprawnej odpowiedzi
- Nie, ponieważ tristearynian glicerolu jest związkiem nasyconym.
- Nie, odbarwienie wody bromowej zaobserwowano tylko w probówce II, ponieważ zawierała tłuszcz nienasycony.
Zadanie 57. (SP17)
Stearyna jest zwyczajową nazwą tristearynianu gliceryny. W temperaturze 25 ºC stearyna jest nierozpuszczalnym w wodzie ciałem stałym. Zmieszano 10 g rozdrobnionej stearyny z 250 cm3 zimnej wody.
Wybierz i podkreśl w każdym nawiasie poprawne uzupełnienie poniższych zdań.
I. Mieszanina rozdrobnionej stearyny i zimnej wody jest (roztworem właściwym / zawiesiną).
II. Składniki opisanej mieszaniny można rozdzielić metodą (krystalizacji / sączenia).
III. Zestaw laboratoryjny, który należy zastosować w tej metodzie, powinien zawierać (lejek z sączkiem / palnik / chłodnicę).
- Mieszanina rozdrobnionej stearyny i zimnej wody jest zawiesiną.
- Składniki opisanej mieszaniny można rozdzielić metodą sączenia.
- Zestaw laboratoryjny, który należy zastosować w tej metodzie, powinien zawierać lejek z sączkiem.
Zadanie 58. (SP17)
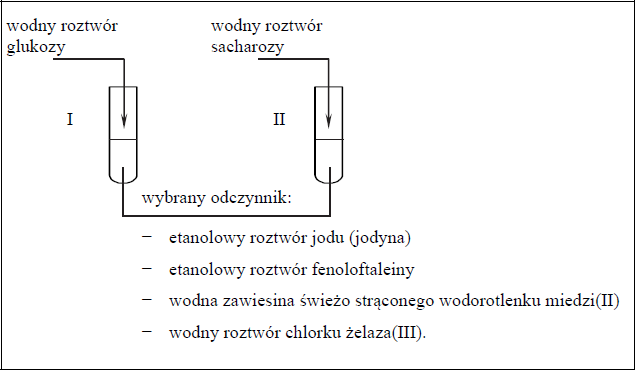
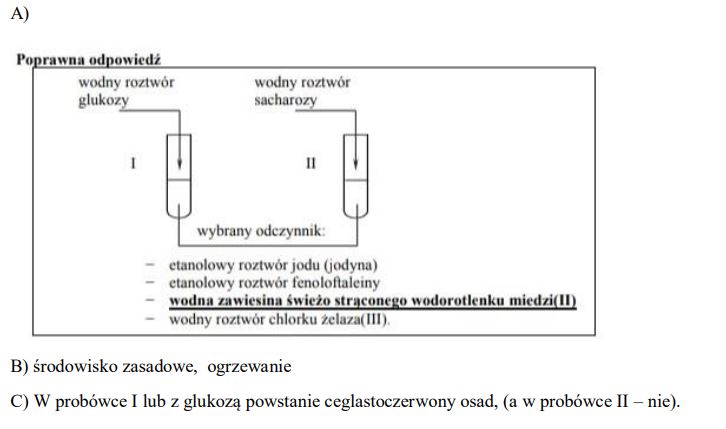
W probówce I umieszczono wodny roztwór glukozy, a probówce II – wodny roztwór sacharozy. Sacharoza, w odróżnieniu od glukozy, nie jest cukrem redukującym.
Zaprojektuj doświadczenie, dzięki któremu można potwierdzić obecność glukozy w roztworze umieszczonym w probówce I i obecność sacharozy w roztworze umieszczonym w probówce II.
a) Uzupełnij schemat doświadczenia. Podkreśl nazwę użytego odczynnika wybranego spośród podanych.
b) Spośród wymienionych poniżej warunków określających środowisko i temperaturę mieszaniny reakcyjnej wybierz te, w których należy przeprowadzić reakcję z wybranym odczynnikiem, i podkreśl nazwy tych warunków.
środowisko kwasowe, środowisko zasadowe, ogrzewanie, chłodzenie
c) Napisz, jakie możliwe do zaobserwowania zmiany zawartości probówki I lub probówki II będą potwierdzeniem obecności glukozy w roztworze znajdującym się w probówce I i obecności sacharozy w roztworze wprowadzonym do probówki II.
Zadanie 59. (SP17)
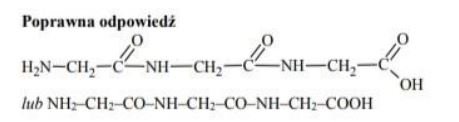
Napisz wzór półstrukturalny (grupowy) tripeptydu powstałego z glicyny o wzorze:
Zadanie 60. (SP17)
Analiza składu pewnego wielkocząsteczkowego związku organicznego naturalnego pochodzenia wykazała, że zawiera on węgiel, wodór, azot, tlen i siarkę. Stwierdzono, że próbka tego związku pod wpływem stężonego wodnego roztworu kwasu azotowego(V) barwi się na żółto. Kolejną próbkę tego związku wprowadzono do probówki z wodą, a następnie wlano tam wodny roztwór wodorotlenku sodu i wodny roztwór siarczanu(VI) miedzi(II). Po wymieszaniu zawartości probówki zaobserwowano powstanie roztworu o barwie fioletowej. Spośród grup związków organicznych, których nazwy wymieniono poniżej, wybierz grupę, do której należy opisany związek, i podkreśl jej nazwę.
Aminokwasy, białka, polisacharydy, tłuszcze
Białka
Zadanie 61. (SP18)
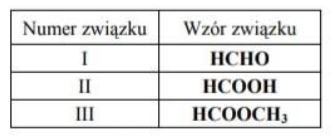
Poniżej przedstawione są wzory sześciu związków organicznych.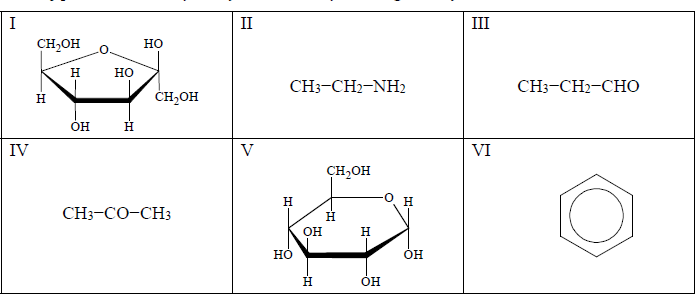
I. Takie same wartości masy molowej mają związki oznaczone numerami ….. i ….. oraz ….. i ……
II. Do węglowodorów aromatycznych zalicza się związek oznaczony numerem ………… .
III. Odczyn zasadowy ma wodny roztwór związku oznaczonego numerem ……………… .
IV. Próbie Trommera i próbie Tollensa ulegają związki oznaczone numerami …………… .
- Takie same wartości masy molowej mają związki oznaczone numerami I i V oraz III i IV.
- Do węglowodorów aromatycznych zalicza się związek oznaczony numerem VI.
- Odczyn zasadowy ma wodny roztwór związku oznaczonego numerem II.
- Próbie Trommera i próbie Tollensa ulegają związki oznaczone numerami I, III, V.
Zadanie 62. (SP18)
Najprostszym aminokwasem jest glicyna o wzorze
a) Podaj nazwy dwóch grup funkcyjnych, które można wyróżnić w cząsteczce
b) Zapisz równanie reakcji glicyny z kwasem chlorowodorowym (solnym). Zastosuj wzory półstrukturalne (grupowe) związków organicznych.
c) Napisz nazwę wiązania utworzonego w wyniku reakcji kondensacji dwóch cząsteczek glicyny.